目前,胃癌仍是我国最常见的恶性肿瘤之一。在自然人群中推行早期胃癌筛查及高危人群进行内镜精查是实现早诊早治、提高治愈率的有效途径。但一直以来,我国一直缺乏针对早期胃癌筛查的可操作性流程,影响了这方面工作的开展。
2017 年底,由国家消化系统疾病临床医学研究中心(上海)李兆申院士牵头,联合多个相关学术委员会,组织了多学科专家,在 2014 版《中国早期胃癌筛查及内镜诊治共识意见》的基础上,结合近年来国内 120 余家医院参与的大数据、多中心临床研究结果,进一步细化并确立了适合我国国情的早期胃癌筛查流程,制定了《中国早期胃癌筛查流程专家共识意见(草案)(2017 年,上海)》。
本文试现将其(下文简称本共识)与 2014 版共识意见相比较,列举其主要的异同之处,以便于大家学习掌握。
一、筛查对象概念的更改
既往筛查对象多采用「高危人群」这一概念,但这一概念容易引起混淆,且使筛查对象产生较大精神压力,因此,本共识意见中筛查对象采用国外常用的「胃癌风险人群」或「胃癌筛查目标人群」的表述。
二、筛查目标人群的范围
本共识仍遵循 2014 版共识的规定,筛查范围为:凡是年龄在 40 岁以上,并且符合下列各项其中之一,属于胃癌风险人群,需要积极进行筛查:
1. 胃癌高发地区人群;
2. 幽门螺杆菌感染者;
3. 患有萎缩性胃炎、胃溃疡、胃息肉、手术后残胃、肥厚性胃炎、恶性贫血等疾病;
4. 胃癌患者的一级亲属(父母、子女、兄弟姐妹);
5. 存在胃癌其他风险因素(高盐、腌制食物、吸烟、重度饮酒等)。
三、筛查方法
1. 血清学检测项目仍推荐 PGⅠ、PGⅡ、PGR、G-17、Hp 抗体等项目,认为能较好地反映胃黏膜萎缩及胃癌发生的风险;
2. 本共识在我国近 15000 例胃癌风险人群研究的结果的基础上,首次提出了适合我国人群的血清学检测临界值。研究表明,当 PGR 低于 3.89,G-17 高于 1.50pmol/L 时,胃癌的发生风险显著增高;
3. 血清肿瘤学标志物方面,常用的 CEA、CA19-9、CA72-4、CA125、CA242 等被认为在早期胃癌中的阳性率极低,因此不推荐作为筛查方法。但本共识首次提出我国自主发现的新型胃癌标志物 MG7 对胃癌诊断的敏感性及特异性均较高,值得进一步研究。MG7 是由西京消化病医院樊代明院士团队发现并深入研究的。
4. 与 2014 版不同的是,对 Hp 感染的检测增加了尿素呼气试验;
5. 内镜检查方面,仍推荐对非侵入性方法筛查出的高风险人群进行有目的的内镜精查策略,而不推荐进行普通人群中大规模内镜筛查。此外,还首次提出了磁控胶囊胃镜系统具有与胃镜相似的敏感性及特异性,是一种可供选择的筛查方式。
6. 否定了上消化道钡餐的价值,不再推荐于胃癌筛查。
四、建立新型胃癌筛查评分系统
本共识的最大亮点是建立了「定量」的风险评分系统,使我国具有了适合中国国情的可操作的风险分层管理方法。该系统包含五个变量,总分 0~23 分,分为三个等级:高危人群(17~23 分)、中危人群(12~16 分)、低危人群(0~11 分)。具体评分方法见下表。
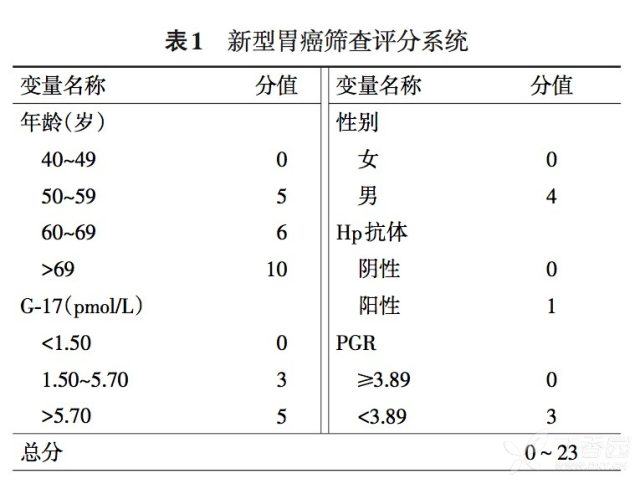
五、建立了早期胃癌筛查流程
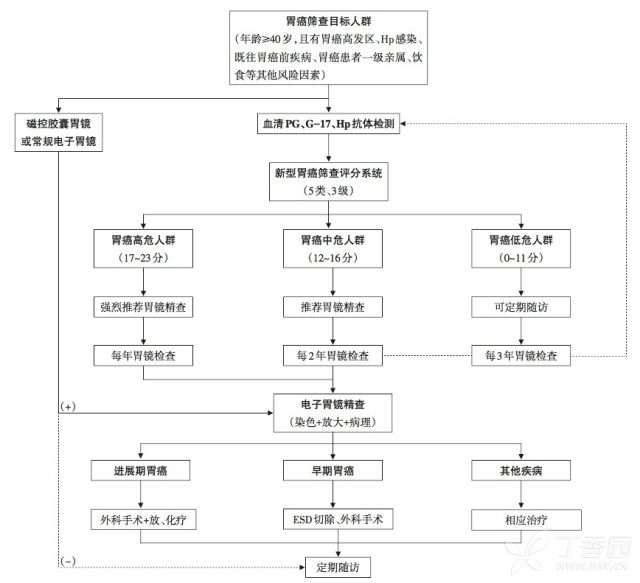
图 1 早期胃癌筛查流程
参考文献
1 李兆申, 等. 中国早期胃癌筛查流程专家共识意见 (草案)(2017 年,上海). 中华健康管理学杂志, 2018, 12(1): 8-14.
2 中国早期胃癌筛查及内镜诊治共识意见 (2014 年, 长沙). 中华消化杂志, 2014, 34(7): 433-448.
3 Tu H, Sun L, Dong X, et al. A Serological Biopsy Using Five Stomach-Specific Circulating Biomarkers for Gastric Cancr Risk Assessment: A Multi-Phase Study. Am G Gastroenterol, 2017,112(5): 704-715.
4 靳斌, 王新, 靳雁, 等. 一种灵敏简便的酶联免疫吸附测定法检测胃癌血清 MG7 抗原. 中华消化杂志, 2016, 36(3): 188-191.
